دیستروفی عضلانی یک بیماری ژنتیک پیشرونده است که خود را با ضعف در قدرت عضلانی و کاهش توده عضلات نشان می دهد. این بیماری به علت نقص در تولید پروتین های مورذ نیاز برای ساخت عضلات ایجاد می گردد. تشخیص دیستروفی های عضلانی دوشن و بکر بر اساس تاریخچه خانوادگی ، یافته های بالینی ، آزمایش های آنزیمی سرم، روش های تشخیص الکتریکی ، نمونه برداری از ماهیچه و روش های مولکولی انجام می گیرد. مرکز دیستروفی عضلانی تهران زیر نظر دکتر صابر در زمینه درمان دیستروفی عضلانی به صورت تخصصی فعالیت می نماید. کاردرمانی در دیستروفی عضلانی بکر و دوشن با استفاده از تجهیزات مکانوتراپی، آب درمانی، ماساژ درمانی و تخصص و تجربه متخصصان کاردرمانی مرکز موجب تسهیل بهبودی و کند شدن روند پیشرفت بیماری می گردد.
روش های تشخیص دیستروفی عضلانی دوشن و بکر
تاریخچه خانوادگی دیستروفی عضلانی دوشن و بکر:
در مورد شیوع دیستروفی اگر خانواده ای با درگیری دیستروفی عضلانی توارث وابسته به کروموزوم X را نشان دهند ، تشخیص DMD و BMD ساده تر خواهد بود . احتمال مشاهده این الگوی وراثتی در خانواده های BMD بیشتر است زیرا مردان مبتلا ازدواج می کنند و دارای فرزند هستند در حالی که نسبت بزرگی از خانواده های DMD نتیجه جهش های جدید می باشند و تشخیص الگوی وراثتی در آنها مشکل است . تشخیص الگوی وراثتی در خانواده هایی که پسران و دختران مبتلا دارند نیز مشکل است زیرا ممکن است بیماری آنها یک اختلال عصبی – عضلانی با توارث اتوزومی مغلوب باشد بنابراین افتراق دیستروفی عضلانی دوشن و بکر از دیگر اختلالات عصبی – عضلانی بر اساس تاریخچه خانوادگی کار چندان آسانی نخواهد بود) .
یافته های بالینی دیستروفی دوشن و بکر:
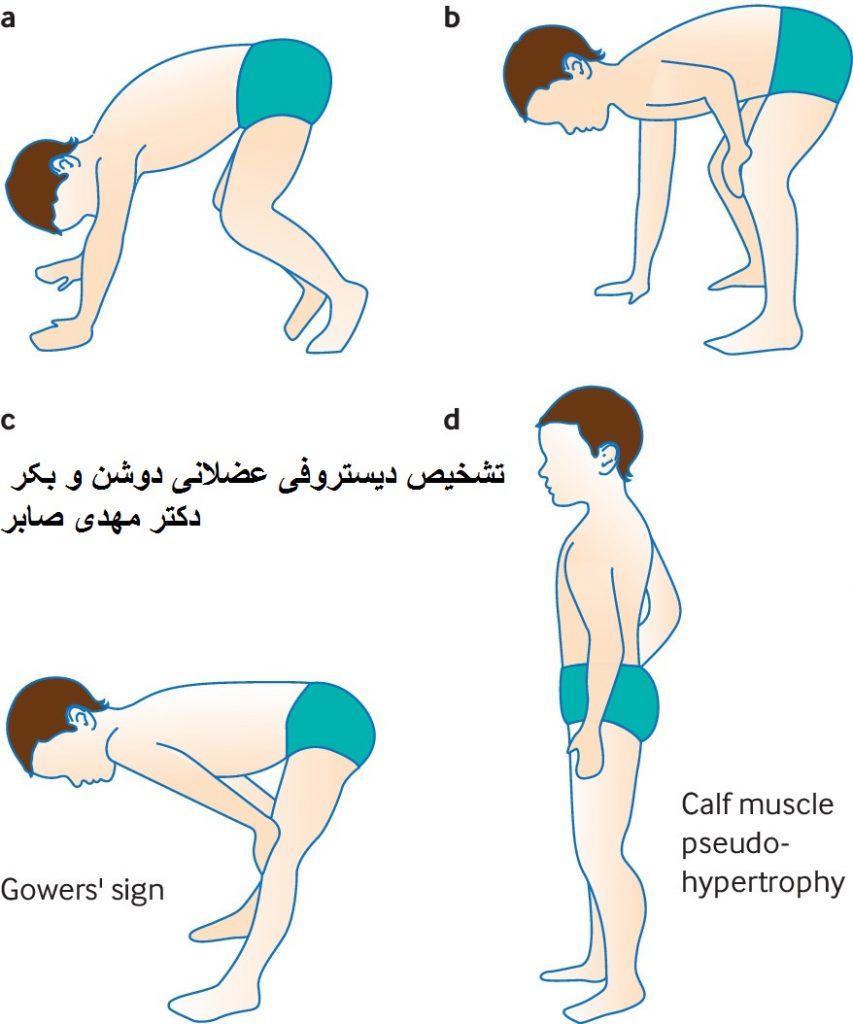
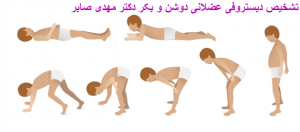
یافته های بالینی نمی تواند در تشخیص نهایی دیستروفی دوشن و بکر راهگشا باشد چرا که علائمی مانند هیپرتروفی کاذب عضلات ساق پا ، کتف بالی ، علامت گاورس ، الگوی ضعف عضلانی تنها محدود به این دو بیماری نمی باشند بلکه دیستروفی شبه دو شن که توارث غیر جنسی مغلوب (AR) دارد نیز این علائم را نشان می دهد و فقط سیر پیشرفت بیماری آهسته تر است . دیستروفی کمربند اندامی نیز بعضی از این علائم را نشان می دهد . بنابراین تنها با توجه به نشانه های بالینی نمی توان به یک تشخیص افتراقی دقیق دست یافت ، هم چنین تشخیص افتراقی دوشن از بکر در سنین قبل از ۱۲ سالگی آسان نیست.
آنزیم های سرمی:
میزان آنزیم های سرمی در دیستروفی های عضلانی مانند هر بیماری عضلانی تغییر می کند . این آنزیم ها شامل آمینوترانسفراز ، آلدولاز (۳) ، لاکتات دهیدروژناز و کراتین کیناز می باشند . این آنزیم ها از رشته های عضلانی آسیب دیده آزاد می شوند که می توان میزان آنها را در سرم اندازه گیری کرد . حساسترین این آنزیم ها در تشخیص دوشن آنزیم کراتین فسفوکیناز( ck یا cpk ) می باشد که فقط در عضلات اسکلتی ، عضله قلب و مغز یافت می شود . در افراد مبتلا به دوشن سطح سرمی این آنزیم ۵۰ تا ۱۰۰ برابر میزان طبیعی افزایش می یابد . سطح سرمی کراتین کیناز در حالت طبیعی ۲۵ تا ۲۰۰ واحد است که در بیماران مبتلا به دوشن به ۱۰۰۰۰ تا ۲۰۰۰۰ واحد می رسد . در بیماران مبتلا به بکر نیز مقدار این آنزیم در خون بالا می رود.
روش های آزمایشگاهی تشخیص دیستروفی بکر
علائم دیستروفی عضلانی بکر می توانند در اوایل کودکی، حتی از 5 سالگی، یا تا 60 سالگی ظاهر شوند. تشخیص دیستروفی عضلانی بکر ممکن است بسیار متفاوت و پیچیده باشد. در واقع، برخی از این بیماران به نقاط عطف رشدی خود نمی رسند و برخی متوجه می شوند که نمی توانند در کلاس های تربیت بدنی یا در طول آموزش نظامی همگام شوند. همانند تشخیص هر نوع دیگری از دیستروفی عضلانی، متخصص معمولاً با گرفتن سابقه بیمار و خانواده اش شروع می کند و سپس یک معاینه فیزیکی جامع انجام می دهد. سابقه و معاینه فیزیکی می تواند تا حد زیادی به تشخیص کمک کند، حتی قبل از انجام هرگونه آزمایش تشخیصی پیچیده. متخصص می خواهد تعیین کند که آیا ضعف بیمار ناشی از مشکلی در خود عضلات است یا در اعصابی که آن ها را کنترل می کنند. مشکلات در اعصاب کنترل کننده عضلات یا در نورون های حرکتی (که از نخاع و مغز منشأ می گیرند و به تمام عضلات بدن می رسند) می توانند ضعفی ایجاد کنند که شبیه یک مشکل عضلانی به نظر می رسد. بیماری های دیگری نیز برخی از علائم مشابه دیستروفی بکر را دارند. دیستروفی عضلانی بکر گاهی اوقات به اشتباه به عنوان دیستروفی عضلانی دوشن یا دیستروفی عضلانی کمربند اندام تشخیص داده شده است. به همین دلیل، انجام یک فرآیند تشخیصی دقیق، که معمولاً شامل آزمایش ژنتیکی (DNA) است، اهمیت دارد. در اوایل فرآیند تشخیصی، پزشکان اغلب یک آزمایش خون خاص به نام سطح CK را تجویز میکنند. CK مخفف کراتین کیناز است، آنزیمی که از عضلات آسیب دیده نشت می کند. هنگامی که سطوح بالای CK در نمونه خون یافت می شود، معمولاً به این معنی است که عضله توسط یک فرآیند غیر طبیعی، مانند دیستروفی عضلانی یا التهاب، در حال تخریب است. بنابراین، سطح بالای CK نشان می دهد که خود عضلات علت احتمالی ضعف هستند، اما دقیقاً نمی گوید که اختلال عضلانی چه می تواند باشد. آزمایش DNA برای تشخیص دیستروفی بکر اکنون به طور گسترده در دسترس است و معمولاً از نمونه خون انجام می شود. در بسیاری از موارد، آزمایش DNA به تنهایی می تواند با درجه بالایی از قطعیت به خانواده ها و پزشکان بگوید که مسیر بیماری به احتمال زیاد دیستروفی عضلانی بکر است یا دوشن. به طور خلاصه، تشخیص دستروفی دوشن و بکر پیچیده است. این شامل تظاهرات بالینی، یافته های آزمایشگاهی، آزمایش ژنتیکی، آزمایش های ابزاری و بیوپسی عضلانی است. اکثر تکنیک های تشخیصی به طور گسترده در دسترس و قابل انجام هستند.
روش های تشخیص الکتریکی دیستروفی عضلانی
برای تشخیص افتراقی بیماری عضلانی ناشی از اختلال عضله و یا اختلال عصب از دو روش الکترومیوگرافی و اندازه گیری سرعت هدایت عصبی استفاده می شود.
با اندازه گیری NCV می توان اختلالات عصبی را از بیماری های ماهیچه ای تفکیک روش الکتروفیزیولوژی و با به کار بردن الکترودهای سطحی می توان هدایت عصبی حرکتی و حسی را اندازه گیری کرد . با تحریک عصبی که عضله را در نقاط مختلف عصب دهی می کند می توان سرعت هدایت را از روی زمان لازم برای انتقال تحریک از هر نقطه تا ایجاد پاسخ عضلانی ، اندازه گیری کرد . سرعت هدایت بستگی به قطر و عمق میلینه بودن عصب دارد . هرگاه سرعت هدایت عصبی کاهش یابد نشانگر وجود نوروپاتی های مختلف است در حالی که در بیماری های عضلانی ، سرعت هدایت عصبی طبیعی است . سرعت هدایت عصبی در نوزادان تازه متولد شده نصف میزان بچه های 3.۵ سال میباشد .
در روش EMG برای ثبت فعالیت الکتریکی عضله ، پتانسیل های الکتریکی را در وضعیت های مختلف انقباضی با فرو بردن یک الکترود سوزنی در داخل عضله ثبت می نمایند . عضله طبیعی در حال استراحت خاموش است ولی غشاهای عضلانی که عصب آنها قطع شده باشد یا بیمار باشند خودبه خود تحریک می شوند و ایجاد پتانسیل های فیبریلاسیون می کنند . یافته های الکترومیوگرافی در بیماری های اولیه عضله مشخص است و ضمن انقباض ارادی عضله ، می توان واحدهای حرکتی کوچک بسیاری را شناسائی نمود که دامنه پتانسیل آنها کاهش یافته است.
فیبریلاسیون و امواج تیز مثبت نیز در بیماران عضلانی ممکن است مشاهده شود . در بیماران مبتلا به دوشن الکترومیوگرام الگوی میوپاتیک دارد و از الگوی مربوط به بیماری های عصبی قابل تفکیک است (۲) در حالی که سرعت هدایت عصبی طبیعی می باشد.
نمونه برداری از عضله جهت تشخیص دیستروفی عضلانی بکر و دوشن :
اختصاصی ترین روش تشخیص در بیماری های عضله قبل از ژنتیک مولکولی نمونه برداری یا بیوپسی عضلانی است . تغییرات بافتی بستگی به مرحله بیماری دارد . با نمونه برداری می توان نوع میوپاتی و میزان پیشرفت بیماری را مشخص کرد.
عضله ای که بیوپسی روی آن انجام می گیرد باید مبتلا باشد اما آسیب وارده به خیلی شدید نباشد . عضله نباید محل تزریق اخیر یا مطالعات EMG با سوزن بوده با و بیشتر مواقع عضله چهار سررانی یا عضله گاستروکنمیوس واقع در ساق پا می باشد . ساختمان بافت ماهیچه ای در دیستروفی های عضلانی و هم چنین در دوشن تغییراتی شامل اختلاف در اندازه رشته های عضلانی ، تخریب رشته ها با فاگوسیتوز و جایگزینی بافت عضلانی توسط بافت همبندی و چربی را نشان می دهد . در برخی رشته های عضلانی ، هسته ها در مرکز قرار گرفته اند و وجود بازوفیلی در فیبرها و فعالیت بازسازی قابل مشاهده است . اصطلاح دیستروفیک که در مورد نمونه بافت شد (۵) عضلانی استفاده می شود به معنای مجموع تغییرات گوناگونی است که از آن ها نام برده شد. درجه تغییرات متفاوت از بیماری به بیمار دیگر همیشه با نمای بالینی ارتباط نزدیکی ندارد . تشخیص افتراقی دوشن از نوع بکر یا کمربند شانه ای بر مبنای بیوپسی مشکل است و باید شدت بیماری و سن بیمار حتما در نظر گرفته شود .
روش ایمونوهسیتوشیمی یا لکه گذاری ایمنی (۷) راه مناسبی برای تشخیص DMD/BMD با انجام بیوپسی عضلات می باشد . با به کارگیری یک آنتی بادی اختصاصی علیه دیستروفین ، می توان به محل قرار گرفتن دیستروفین در غشا سلول های عضله طبیعی ، کاهش مقدار دیستروفین در عضله مبتلا BMD و فقدان کامل آن در عضله مبتلا به DMD پی برد . در روش لکه گذاری ایمنی فقدان دیستروفین به طور وضوح مشخص است در حالی که تغییرات دیستروفین در BMD با پراکندگی رنگ به طور ناهمگون یا کاهش رنگ آمیزی همراه است . بنابراین روش لکه گذاری ایمنی که قابلیت تشخیص تغییرات دیستروفین از نظر اندازه و هم چنین قابلیت تشخیص تغییرات و آن را دارد برای شناسائی BMD روش مفیدتری است . بیماران BMD در ۸۶٪ موارد تغییر در اندازه دیستروفین دارند در حالی که فقط ۹٪ آنها کاهش در مقدار دیستروفین را نشان میدهند.
منابع:
mda.org
mj.tbzmed.ac.ir
سوالات متداول:
1.آیا برای تشخیص دیستروفی عضلانی نیاز به آزمایش است؟
بله، تشخیص دیستروفی عضلانی در مرحله اول با مشاهده علائم توسط پزشک و کسب تاریخچه خانوادگی آغاز می گردد، سپس برای تایید تشخیص آزمایش خون و نمونه برداری از بافت عضلات انجام می گیرد.
2.برای تشخیص افتراقی دیستروفی عضلانی دوشن و بکر چکار باید کرد؟
اختصاصی ترین روش تشخیص در بیماری های عضله قبل از ژنتیک مولکولی نمونه برداری یا بیوپسی عضلانی است . تغییرات بافتی بستگی به مرحله بیماری دارد . با نمونه برداری می توان نوع میوپاتی و میزان پیشرفت بیماری را مشخص کرد.